1404/10/02 21:24:18
ریتالین :آنچه درمانگران و والدین باید بدانند 2
شروع درمان و تیترهکردن دوز (Initiation and Titration)
بهطور کلی، کارآزماییهای بالینی تصادفیشده و کنترلشده (RCT) برتری ثابت و مشخصی را برای یک فرمولاسیون محرک نسبت به سایرین نشان ندادهاند؛ بنابراین به پزشکان توصیه میشود درمان را با داروهای محرکی که شواهد علمی معتبر و گستردهتری دارند آغاز کنند.
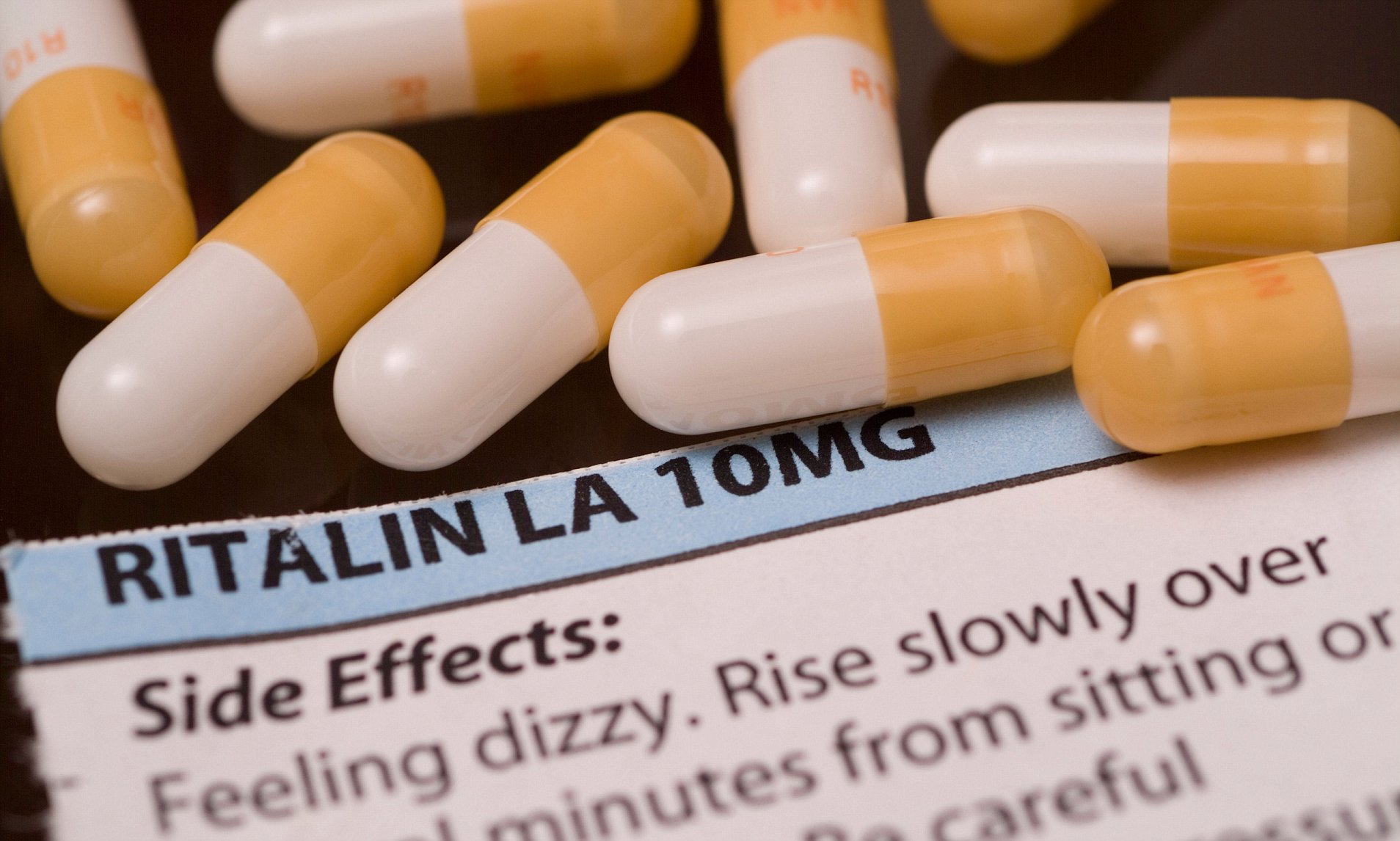
راهنمای دارویی ADHD (ADHD Medication Guide) که بهصورت آنلاین توسط Cohen Children’s Center ارائه شده است، بهطور منظم بهروزرسانی میشود و شامل تصاویر قرصها برای شناسایی آسانتر نیز هست.
در عمل بالینی رایج، درمان با یکی از فرآوردههای متیلفنیدات یا آمفتامین از کمترین دوز ممکن شروع میشود و سپس دوز دارو در ویزیتهای بعدی (مثلاً ماهانه یا هر چند ماه یکبار) بر اساس گزارش والدین، معلمان و/یا خود بیمار از پاسخ درمانی و عوارض جانبی، بهتدریج افزایش (تیتره) مییابد.
با این حال، والدینی که نسبت به مصرف دارو تا حدی نگرانی یا تردید دارند، ممکن است خیلی زود به بهبودهای ناکافی با دوز پایین رضایت دهند؛ حتی در شرایطی که اختلال عملکرد ناشی از علائم ADHD همچنان ادامه دارد.
در مقایسه با مراقبتهای معمول جامعه (اصطلاحاً care as usual)، پروتکلهای تیترهکردن محرکها که از مقیاسهای درجهبندی استاندارد والدین و معلمان در فواصل منظم و برنامهریزیشده (هفتگی تا ماهانه) استفاده میکنند، در محیطهای پژوهشی اغلب به دستیابی سریعتر به دوز بهینه و اثربخشی مطلوبتر منجر شدهاند.
پزشک ممکن است هنگام شروع درمان با داروی محرک، از یک برنامه تیتره تهاجمیتر (مثلاً «دوزگذاری اجباری» یا forced-dose titration) استفاده کند. یکی از این روشها آن است که ۳۰ کپسول از یک دارو تجویز شود و از بیمار خواسته شود سه دوز متفاوت را، هر کدام به مدت ۵ روز امتحان کند و سپس پس از ۲ هفته پیگیری انجام شود.
برای مثال، میتوان ۳۰ کپسول دکسمتیلفنیدات با رهش طولانیاثر ۵ میلیگرمی تجویز کرد و دستور داد:
۵ روز: روزانه ۱ کپسول (۵ میلیگرم)
۵ روز: روزانه ۲ کپسول (۱۰ میلیگرم)
۵ روز: روزانه ۳ کپسول (۱۵ میلیگرم)
در صورتی که عوارض جانبی قابلتوجهی ایجاد شود و بیش از چند روز ادامه یابد، میتوان تیترهکردن را متوقف کرد. در ویزیت پیگیریِ ۲ هفتهای، پزشک و مراقب کودک میتوانند تصمیم بگیرند که کدام دوز مناسبتر است.
اگر انتخاب اولیه داروی محرک از نظر تعادل سود و زیان رضایتبخش نباشد، توصیه میشود داروی محرک دیگری مورد آزمایش قرار گیرد. مطالعات نشان دادهاند که حدود ۷۵ تا ۸۰ درصد افراد مبتلا به ADHD به متیلفنیدات یا آمفتامین پاسخ درمانی مناسب میدهند.
– عوارض جانبی (Side Effects)
تمام داروهای محرک (Stimulant medications) از نظر کلی پروفایل عوارض جانبی مشابهی دارند؛ هرچند تجربه هر بیمار میتواند بسته به نوع دارو، فرمولاسیون و دوز مصرفی متفاوت باشد. بروز عوارض جانبی قابلتوجه با یک فرآورده خاص در یک کلاس دارویی محرک (مثلاً متیلفنیدات methylphenidate) لزوماً به این معنا نیست که امتحان یک فرآورده دیگر از همان کلاس دارویی امکانپذیر یا قابلتحمل نخواهد بود.
عوارض جانبی شایع شامل سردرد، دلدرد، افزایش خفیف ضربان قلب یا فشار خون، کاهش اشتها و دشواری در شروع خواب است. سردرد و دلدرد ممکن است با سازگاری تدریجی بدن با دارو بهطور خودبهخود برطرف شوند و همچنین در صورت مصرف دارو همراه با غذا بهبود یابند.
مشکل در شروع خواب معمولاً با گذشت زمان برطرف نمیشود و اغلب به طول اثر دارو یا به پدیده بازگشت علائم (rebound) پس از پایان اثر دارو مربوط است.
تحریکپذیری (irritability) و بینظمی خلقی (mood dysregulation) نیز ممکن است رخ دهند که اغلب در اواسط تا اواخر بعدازظهر یا اوایل عصر و همزمان با کاهش اثر دارو مشاهده میشوند. این عوارض ناخواسته دارویی، در صورتی که بر منافع درمانی برای کودک غلبه کنند، میتوانند تحملپذیری دارو را محدود نمایند.
در چنین شرایطی، پزشک میتواند بهجای قطع کامل درمان، با تنظیم رژیم دارویی (تغییر دوز، زمان مصرف یا نوع فرمولاسیون) تلاش کند عوارض جانبی را به حداقل برساند.
ترجمه متن:
عوارض جانبی غیرشایع (Uncommon Side Effects)
عوارض جانبی غیرشایع درمان با داروهای محرک شامل روانپریشی القاشده توسط محرکها (توهمهای بینایی، شنوایی یا لمسی، یا افکار سایکوتیک)، پرخاشگری، بیمهاری رفتاری و/یا مانیا است. این عوارض معمولاً در دوزهای بالا یا در افرادی که زمینه ابتلا به اسکیزوفرنی یا اختلال دوقطبی دارند، مشاهده میشوند. اثر موسوم به «زامبی» که گاهی توسط والدین توصیف میشود نیز اغلب با دوز بیش از حد دارو مرتبط است.
رابطه بین مصرف طولانیمدت داروهای محرک و رشد کودک پیچیده است. نگرانی اصلی همواره کاهش افزایش وزن و احتمال تأثیر بر دستیابی به قد نهایی بزرگسالی بوده که عمدتاً به دلیل کاهش دریافت کالری ناشی از مهار اشتها مطرح میشود. با این حال، مکانیسمهای دیگری نیز پیشنهاد شدهاند؛ از جمله تأثیر محرکها بر تنظیم مرکزی رشد در سیستم عصبی مرکزی، تغییرات ایجادشده در متابولیسم کبدی، و تغییرات غضروفی.
شواهد جدید نشان میدهد که هرگونه اثر منفی بر رشد، احتمالاً بیشتر بر سرعت رشد تأثیر میگذارد (به این معنا که کودکان در نهایت به قد واقعی بزرگسالی خود میرسند) یا اینکه این اثرات خفیف، وابسته به دوز، و برگشتپذیر پس از قطع دارو هستند.
اقداماتی که در عمل بالینی برای کاهش اثرات منفی بر وزن و قد انجام میشوند شامل افزایش دریافت کالری، استفاده از محرکهای اشتها (مانند سیپروهپتادین) و تعطیلات دارویی (drug holidays) در آخر هفتهها یا تعطیلات هستند؛ با این حال، پشتوانه پژوهشی قوی برای این روشها وجود ندارد. هنگام تصمیمگیری برای کاهش دوز، وقفه یا قطع درمان دارویی به دلیل اثرات بر وزن، پزشک باید منافع بالقوه دارو بر عملکرد تحصیلی، اجتماعی و رفتاری کودک را نیز مدنظر قرار دهد.
برای مثال، هیچ اندیکاسیونی برای قطع داروهای محرک در تابستان صرفاً بهمنظور «استراحت دادن به مغز» وجود ندارد.
رابطه تیکها با مصرف داروهای محرک در ADHD
رابطه بین تیکها (Tics) و مصرف داروهای محرک همواره موضوع بحث و اختلافنظر بوده است. اگرچه در گذشته این نگرانی وجود داشت که داروهای محرک ممکن است باعث تشدید تیکها شوند، اما باید توجه داشت که تیکها بهطور طبیعی نوساندار (wax and wane) هستند و افزایش دفعات آنها ممکن است ناشی از سیر طبیعی اختلال باشد، نه الزاماً مصرف دارو.
در حال حاضر، وجود همزمان اختلال تیک و ADHD دیگر بهعنوان منع مصرف (contraindication) داروهای محرک تلقی نمیشود. با این حال، اگر در جریان درمان، تیکهای گذرا ایجاد شوند یا تیکها بهطور واضح تشدید شوند، ممکن است نیاز به تغییر درمان دارویی وجود داشته باشد.
در چنین شرایطی، برخی پزشکان از روش آزمون قطع و وصل دارو بهصورت ABAB استفاده میکنند؛ به این معنا که دارو بهطور برنامهریزیشده قطع و سپس دوباره شروع میشود تا تأثیر آن بر فراوانی و شدت تیکها بهدقت بررسی شود.
عوارض قلبی داروهای محرک: واقعیتها و توصیههای بالینی
در سالهای اخیر، نگرانیهایی درباره عوارض قلبی داروهای محرک مطرح شده است. مطالعات نشان دادهاند که این داروها ممکن است باعث افزایش خفیف فشار خون سیستولیک (حداکثر تا ۷ میلیمتر جیوه) و افزایش ضربان قلب (تا ۱۰ ضربه در دقیقه) شوند. حدود ۵ تا ۱۵ درصد از افراد تحت درمان ممکن است افزایشهای قابلتوجهتری را تجربه کنند (مانند فشار سیستولیک ≥۱۲۰ میلیمتر جیوه، افزایش فشار سیستولیک ≥۲۰ میلیمتر جیوه، یا افزایش ضربان قلب ≥۲۰ ضربه در دقیقه)، که این تغییرات معمولاً گذرا هستند.
با این حال، در اوایل دهه ۲۰۰۰ میلادی، گزارشهایی از مرگ ناگهانی در افرادی که داروهای محرک مصرف میکردند منتشر شد و نگرانیهایی درباره اثر آریتموژنیک این داروها ایجاد کرد. در سال ۲۰۰۵، سازمان غذا و داروی آمریکا (FDA) هشداری را به ترکیبات آمفتامینی اضافه کرد مبنی بر اینکه «مرگ ناگهانی در کودکان مبتلا به ناهنجاریهای ساختاری قلب که با دوزهای معمول آمفتامین درمان شدهاند، گزارش شده است».
در ماه مه ۲۰۰۸، انجمن قلب آمریکا (AHA) توصیه کرد که تمام بیماران مبتلا به ADHD که کاندید دریافت داروهای محرک هستند، باید از نظر نقایص قلبی احتمالی بهدقت ارزیابی شوند. این ارزیابی شامل موارد زیر است:
شرح حال دقیق خانوادگی (سابقه مرگ ناگهانی، آریتمیها، بیماریهای قلبی)
بررسی علائم قلبی خفیف در کودک یا نوجوان (مانند تپش قلب، سنکوپ، درد قفسه سینه هنگام فعالیت)
معاینه کامل قلب
در نظر گرفتن نوار قلب (ECG) غربالگری، ترجیحاً با تفسیر کاردیولوژیست اطفال
در آگوست ۲۰۰۸، آکادمی اطفال آمریکا (AAP) و AHA در بیانیهای مشترک تأکید کردند که انجام ECG غربالگری اقدامی قابلقبول ولی الزامی نیست و این نکته مهم را مطرح کردند که:
«درمان بیمار مبتلا به ADHD نباید صرفاً به دلیل انجام نشدن ECG به تعویق بیفتد یا متوقف شود.»
در عمل بالینی امروزی، بهطور کلی ارجاع به متخصص قلب برای شروع داروی محرک تنها در صورتی ضروری است که یافتههای نگرانکنندهای در شرح حال فردی، سابقه خانوادگی یا معاینه فیزیکی وجود داشته باشد. توصیه میشود پزشکان پیش از شروع درمان با داروهای محرک، یافتههای منفی مهم (pertinent negatives) را بهطور دقیق در پرونده پزشکی بیمار ثبت کنند.
آگونیستهای آلفا-۲ (Alpha-2 Agonists) در درمان ADHD
آگونیستهای آلفا-۲ (Alpha-2 agonists) که بهصورت کلونیدین (Clonidine) و گوانفاسین (Guanfacine) در دسترس هستند، اثربخشی قابلقبولی در درمان بیشفعالی (Hyperactivity) و بیتوجهی (Inattention) نشان دادهاند.
مکانیسم اثر (Mechanism of Action)
کلونیدین نخستینبار در دهه ۱۹۶۰ میلادی برای درمان پرفشاری خون توسعه یافت و بر گیرندههای آلفا-۲ نوع 2A، 2B و 2C در قشر پیشپیشانی مغز (Prefrontal Cortex) اثر میگذارد.
گوانفاسین در اواخر قرن بیستم معرفی شد و بهطور اختصاصیتر به گیرنده آلفا-۲A متصل میشود؛ به همین دلیل اثر کمتری بر فشار خون دارد.
گیرندههای آلفا-۲ در قشر پیشپیشانی نقش مهمی در حفظ توجه و تمرکز دارند. اگرچه مکانیسم دقیق اثر این داروها بهطور کامل مشخص نیست، اما فرض بر این است که آگونیستهای آلفا-۲ باعث افزایش انتقال دوپامین و نوراپینفرین در این ناحیه میشوند؛ البته از مسیری متفاوت با داروهای محرک (Stimulants).
وضعیت تأیید FDA و کاربرد بالینی
آگونیستهای آلفا-۲ تا اوایل قرن ۲۱ میلادی بهصورت off-label برای درمان ADHD استفاده میشدند، تا اینکه FDA در سالهای ۲۰۰۹ و ۲۰۱۰ استفاده از آنها را برای کودکان ۶ سال و بالاتر تأیید کرد.
نکات مهم:
فقط فرمهای طولانیاثر (Extended-release) کلونیدین و گوانفاسین دارای تأیید FDA هستند:
با این حال، در عمل بالینی، استفاده off-label از فرمهای کوتاهاثر (Immediate-release) کلونیدین و گوانفاسین شایع است.
اگرچه این داروها برای سایر اختلالات روانپزشکی تأیید نشدهاند، گاهی در درمان:
اثربخشی و جایگاه درمانی
مطالعات نشان دادهاند که آگونیستهای آلفا-۲ طولانیاثر در کاهش علائم ADHD مؤثر هستند.
اندازه اثر (Effect size) این داروها حدود ۰٫۷ است که متوسط محسوب میشود، اما از اندازه اثر داروهای محرک (حدود ۱٫۰) کمتر است.
اثر درمانی فوری نیست و معمولاً ۲ تا ۴ هفته زمان لازم است تا بهطور بالینی آشکار شود.
بر این اساس، راهنماهای بالینی آکادمی اطفال آمریکا (AAP) و آکادمی روانپزشکی کودک و نوجوان آمریکا (AACAP)، آگونیستهای آلفا-۲ را بهعنوان درمان خط دوم (Second-line therapy) طبقهبندی میکنند.
موارد اندیکاسیون مهم
آگونیستهای آلفا-۲ ممکن است در شرایط زیر انتخاب مناسبی باشند:
کودکانی که تحمل هیچیک از داروهای محرک را ندارند
استفاده بهعنوان درمان خط اول در کودکان مبتلا به ADHD همراه با اختلال طیف اوتیسم (ASD)، بهدلیل احتمال بالاتر بروز عوارض محرکها در این جمعیت
کمک به کنترل رفتارهای مقابلهای و نافرمانی در کودکان مبتلا به ADHD
(اگرچه همچنان داروهای محرک درمان خط اول باقی میمانند)
نقش آگونیستهای آلفا-۲ در درمان ترکیبی ADHD
آگونیستهای آلفا-۲ علاوه بر تکدرمانی، در درمان ترکیبی (Combination therapy) نیز نقش مهمی دارند. این داروها بهویژه زمانی مفید هستند که کودک تحمل افزایش دوز داروی محرک را ندارد، اما همچنان بهدلیل علائم اختلال نقص توجه/بیشفعالی (ADHD) دچار اختلال عملکرد است.
مزایای بالینی در درمان ترکیبی
برخلاف داروهای محرک، آگونیستهای آلفا-۲ معمولاً پوشش درمانی یکنواختتری در طول روز ایجاد میکنند و میتوانند بهویژه برای کودکانی مفید باشند که:
در بعدازظهر یا عصر دچار تشدید مشکلات توجه میشوند
(زمانی که اثر داروی محرک کاهش یافته یا از بین رفته است)
مبتلا به ADHD همراه با تیکهای حرکتی یا صوتی هستند
(اگرچه همچنان داروهای محرک درمان خط اول محسوب میشوند، حتی در حضور تیک)
دچار اختلالات خواب هستند و بهویژه مشکل شروع خواب دارند
دوز شروع و تنظیم (Titration) آگونیستهای آلفا-۲
فرمهای کوتاهاثر (Immediate-release)
فرمهای کوتاهاثر معمولاً دو بار در روز تجویز میشوند. توصیههای عملی عبارتاند از:
شروع با دوز شبانه برای کاهش عوارض اولیه:
ادامه این دوز بهمدت ۳ تا ۷ روز برای تطابق بدن با دارو
سپس افزایش دفعات مصرف به دو بار در روز
افزایش دوز بهصورت پلهای هر ۳ تا ۷ روز تا رسیدن به بیشترین دوز قابلتحمل
نکات مهم:
فرمهای طولانیاثر (Extended-release)
فرمهای طولانیاثر نیز باید بهصورت تدریجی و مرحلهای تنظیم شوند:
دفع دارو
آگونیستهای آلفا-۲ عمدتاً از طریق ادرار دفع میشوند؛ بنابراین در بیماران با مشکلات کلیوی، توجه بالینی بیشتری لازم است.
جمعبندی بالینی
آگونیستهای آلفا-۲:
گزینهای مؤثر در درمان کمکی ADHD هستند
برای کودکان با عدم تحمل دوزهای بالاتر محرکها بسیار کاربردیاند
در ADHD همراه با تیک یا اختلال خواب ارزش درمانی ویژهای دارند
نیازمند شروع با دوز پایین و افزایش تدریجی هستند تا عوارض کاهش یابد
درمان ترکیبی ADHD
کلونیدین در ADHD
گوانفاسین و بیشفعالی
ADHD و تیک
داروهای غیرمحرک ADHD
اختلال خواب و ADHD
Alpha-2 agonist ADHD
دوزبندی و عوارض جانبی آگونیستهای آلفا-۲ در ADHD
مشابه داروهای محرک، دوزبندی آگونیستهای آلفا-۲ معمولاً بیشتر تحتتأثیر عوارض جانبی محدود میشود تا اهداف مبتنی بر وزن (اگرچه دوزهای متوسط و حداکثر در جدول 23.2 ذکر شدهاند).
عوارض شایع
شایعترین عوارض جانبی آگونیستهای آلفا-۲ عبارتاند از:
خستگی (Fatigue)
سدیشن (Sedation)
خوابآلودگی (Somnolence)
بروز این عوارض در کلونیدین (Clonidine) بیش از گوانفاسین (Guanfacine) گزارش شده است. این عوارض وابسته به دوز هستند و ممکن است با گذشت زمان و تطابق بدن با دارو کاهش یابند؛ بااینحال، اگر طی هفته اول بهبودی مشاهده نشود، احتمال برطرف شدن آنها در ادامه کم است.
در بیمارانی که از فرمهای کوتاهاثر (Immediate-release) استفاده میکنند، تغییر به فرم طولانیاثر (Extended-release)—بهویژه در صورت امکان مصرف شبانه—میتواند به کاهش سدیشن کمک کند.
عوارض آنتیکولینرژیک
برخی عوارض آنتیکولینرژیک (Anticholinergic effects) نیز ممکن است دیده شوند، از جمله:
ایمنی قلبی–عروقی
نگرانیهایی درباره طولانی شدن فاصله QT (QT prolongation)—بهویژه در مورد گوانفاسین—مطرح شده است؛ اما متاآنالیز دادههای موجود وقوع رویدادهای بالینی معنیدار را نشان نداده و بنابراین انجام ECG غربالگری توصیه نمیشود.
آگونیستهای آلفا-۲ ممکن است باعث کاهش خفیف فشار خون سیستولیک و دیاستولیک شوند؛ این تغییرات در جمعیت کودکان معمولاً جزئی و بدون اهمیت بالینی هستند.
قطع ناگهانی و سندرم ترک
قطع ناگهانی آگونیستهای آلفا-۲—بهویژه در دوزهای بالا—میتواند موجب سندرم ترک (Withdrawal syndrome) شود که شامل موارد زیر است:
افزایش فشار خون
سردرد
لرزش
بیقراری
تهوع
توصیه بالینی: هنگام قطع دارو، دوز باید بهصورت تدریجی (Tapering) کاهش یابد و تنظیمات دوز هر ۳ تا ۷ روز انجام شود.
جمعبندی بالینی
دوزبندی آگونیستهای آلفا-۲ عمدتاً بر اساس تحمل عوارض تنظیم میشود.
سدیشن و خوابآلودگی شایعترین محدودکنندههای دوز هستند.
فرمهای طولانیاثر میتوانند تحملپذیری را بهبود دهند.
قطع تدریجی برای پیشگیری از سندرم ترک ضروری است.
عوارض کلونیدین در ADHD
عوارض گوانفاسین کودکان
دوزبندی آگونیست آلفا-۲
QT prolongation گوانفاسین
قطع تدریجی کلونیدین
درمان غیرمحرک ADHD
جدول 23.2. داروهای غیرمحرک (Nonstimulant) مورد استفاده در درمان ADHD
داروهای غیرمحرک مورد تأیید FDA برای درمان ADHD
| نام دارو (ژنریک) | نام تجاری | مدت اثر | اشکال دارویی و نحوه مصرف | دوز اطفال |
|---|
| اتوموکستین (Atomoxetine) | Strattera | 10 تا 12 ساعت | کپسولهای 10، 18، 25، 40، 60، 80، 100 میلیگرم
مصرف بهصورت کامل بلعیده شود | وزن <70 کیلوگرم: شروع با 0.5 mg/kg/day
وزن ≥70 کیلوگرم: 40 mg/day
حداکثر: 1.4 mg/kg/day یا 100 mg/day |
| گوانفاسین طولانیاثر (Guanfacine ER) | Intuniv | 12 ساعت | قرصهای طولانیاثر 1، 2، 3، 4 میلیگرم
مصرف بهصورت کامل بلعیده شود | شروع (≥6 سال): 1 mg/day
حداکثر: 4 mg/day |
| کلونیدین طولانیاثر (Clonidine ER) | Kapvay | 12 ساعت | قرصهای طولانیاثر 0.1 میلیگرم
مصرف بهصورت کامل بلعیده شود | شروع (≥6 سال): 0.1 mg/day
حداکثر: 0.4 mg/day |
داروهای غیرمحرک بدون تأیید FDA برای درمان ADHD (Off-label)
| نام دارو (ژنریک) | نام تجاری | مدت اثر | اشکال دارویی و نحوه مصرف | دوز اطفال |
|---|
| کلونیدین (Clonidine) | Catapres | طبق بروشور دارو | قرصهای 0.1، 0.2، 0.3 میلیگرم یا سیستم ترانسدرمال (چسب پوستی)
قرصها کامل بلعیده شوند؛ پس از رسیدن به دوز خوراکی پایدار، میتوان به دوز معادل ترانسدرمال تغییر داد | وزن <45 کیلوگرم: شروع 0.05 mg/day
وزن ≥45 کیلوگرم: 0.1 mg/day
حداکثر: 0.4 mg/day در دوزهای منقسم |
| گوانفاسین (Guanfacine) | Tenex | طبق بروشور دارو | قرصهای 1 و 2 میلیگرم
قرصها کامل بلعیده شوند؛ در صورت تغییر از فرم سریعاثر (IR)، ابتدا IR قطع و ER با 1 mg/day شروع شود | وزن <45 کیلوگرم: شروع 0.5 mg/day
وزن ≥45 کیلوگرم: 1 mg/day
حداکثر: 4 mg/day |
اختصارات
نکات کلینیکی کوتاه
داروهای غیرمحرک گزینه مهمی در کودکانی هستند که تحمل داروهای محرک را ندارند.
اتوموکستین تنها داروی غیرمحرک با دوزبندی مبتنی بر وزن است.
گوانفاسین ER و کلونیدین ER بهویژه در ADHD همراه با تیک، اختلال خواب یا ASD کاربرد دارند.
قطع ناگهانی آگونیستهای آلفا-۲ توصیه نمیشود و باید تدریجی انجام شود.
داروهای غیرمحرک ADHD
دوز اتوموکستین کودکان
گوانفاسین ER در ADHD
کلونیدین ADHD اطفال
درمان غیرمحرک بیشفعالی